產品搜索
聯系我們
電話:4008750250
手機:18066071954
地址:南京市棲霞區緯地路9號
Email: zhangxiangwen@cobioer.com
新聞動態 / news
基因療法研究進展一覽
原載自:www.diyiqukuai.com.cn[行情動態] 2017-07-28 瀏覽次數:1624
本期為大家帶來的是基因與人類疾病相關領域的研究進展,希望讀者朋友們能夠喜歡。

1. Retrovirology:整合到人基因組中的古老逆轉錄病毒有助抵抗HIV-1感染
doi:10.1186/s12977-017-0351-8
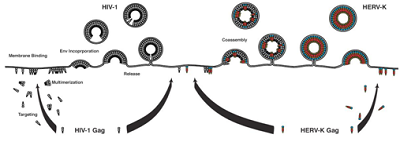
在我們的進化過程中,病毒持續地感染人體。一些早期的病毒已整合到我們的基因組中,如今它們被稱作為人內源性逆轉錄病毒(human endogenous retroviruses, HERV)。在上百萬年來,它們因它們的遺傳密碼發生突變或較大的缺失而變得沒有活性。如今,作為研究得zui多的HERV家族之一是HERV-K家族,該家族自從人類和黑猩猩在進化上分開以來就變得活躍,而且它的一些成員在過去幾十萬年里可能活躍地感染人類。
HERV成為HIV研究人員的關注目標是因為已有研究證實在那些HIV感染者中,T細胞產生抵抗HERV的免疫反應。如今,據認為HERV表達是由HIV感染導致的,而且通過靶向HERV抗原而不是不斷發生突變的HIV抗原,HIV將變成一種更容易的靶標。在提出這種看法之后,日本熊本大學之前開展的一項研究已揭示出HIV-1組特異性抗原(group specific antigen, Gag)和HERV-K Gag共組裝與HIV-1顆粒增殖能力和感染性下降存在明顯的關聯性。在當前的一項新的研究中,來自熊本大學的這些研究人員尋求闡明HERV-K Gag如何以這種方式影響HIV-1。
他們報道在早期的共組裝階段,HERV-K Gag改變后代HIV-1顆粒的大小和形態。這發生的原因在于HERV-K Gag衣殼(即HERV-K病毒蛋白衣殼)部分上與HIV-1 Gag在細胞膜上共定位(或者說重疊)。這也會導致成熟的HIV-1顆粒數量下降、HIV-1更慢地釋放和感染性下降。相關研究結果近期發表在Retrovirology期刊上,論文標題為"Molecular mechanisms by which HERV-K Gag interferes with HIV-1 Gag assembly and particle infectivity"。
論文通信作者、熊本大學生命科學學院微生物學系項目Kazuaki Monde博士說,"盡管我們發現HIV-1顆粒的釋放效率和感染性受到HERV-K Gag的阻礙,但是它們似乎是由兩種不同的機制導致的。也表達HERV-K Gag的細胞釋放HIV-1顆粒的能力顯著下降,但是HIV-1感染性如何也會下降的細節仍然讓我們困惑。當然,還需針對HERV-K Gag衣殼開展更多的研究以便確定它如何能夠降低HIV-1顆粒釋放和感染性。"
2. Cell:zui大規模基因功能分析揭示出很多潛在的抗瘧疾藥物靶標
doi:10.1016/j.cell.2017.06.030
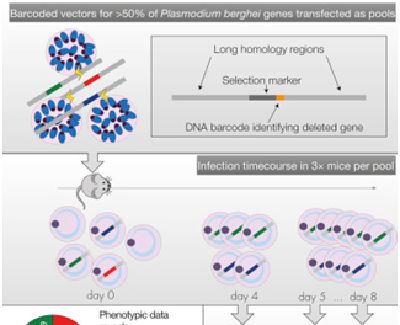
在對瘧原蟲基因功能的*有史以來大規模的研究中,來自英國韋爾科姆基金會桑格研究所等研究機構的研究人員發現瘧原蟲的成功歸結于將它的基因組縮小到僅由必需基因組成。他們分析了這種瘧原蟲基因組中的一半以上的基因,結果發現三分之二的這些基因是它的存活所*的。這也是迄今為止在研究過的任何一種有機體中發現的zui大比例的必需基因。這些結果鑒定出很多潛在靶標可用于新的抗瘧疾藥物開發。對于這種很少理解的存在嚴重耐藥性問題的瘧原蟲而言,這是一項重大的發現。相關研究結果發表在2017年7月13日的Cell期刊上,論文標題為"Functional Profiling of a Plasmodium Genome Reveals an Abundance of Essential Genes"。
瘧原蟲的基因功能是很難理解的。它是古老的有機體,而且它的大約一半的基因在任何其他的有機體中沒有同源基因,這就使得科學家們很難發現關于它們的功能的線索。這項研究是迄今為止提供證據證實了大多數的這些基因的功能。
科學家們已研究了一種被稱作伯氏瘧原蟲(Plasmodium berghei)的瘧原蟲的基因,這些基因在它的復雜的多階段生命周期的單個血液階段中表達。在這項新的研究中,這些研究人員設計出一種新的方法來破譯這種瘧原蟲的基因功能。他們敲除了2578個基因(占這種瘧原蟲基因組的一半以上),然后給每種基因敲除設計一個*的DNA條形碼。
這些研究人員隨后利用下一代基因組測序技術對這些條形碼進行計數,因而測量了每個基因修飾的瘧原蟲蟲株的生長。如果被敲除的基因不是必需的,那么這種瘧原蟲數量激增,但是如果被敲除的基因是必需的,那么這種瘧原蟲就會消失。
這些研究人員系統性地證實這種瘧原蟲能夠很容易地清除所編碼的蛋白會讓宿主免疫系統知道它的存在的基因。這就給開發瘧疾疫苗帶來問題,這是因為這種瘧原蟲能夠很快地改變它的外觀來逃避人免疫系統的檢測,也因此它能夠對瘧疾疫苗產生抵抗性。
這項研究發現了更多*的瘧疾藥物靶標。zui高目標就是發現在這種瘧原蟲生命周期的所有階段都是必需的基因。如果人們能夠利用藥物靶向這些基因,那么就會讓瘧原蟲無處可逃。
3. Genome Biol:科學家利用新型技術繪制基因圖譜 有望改善癌癥診斷
DOI: 10.1186/s13059-017-1253-8

基因組結構的大規模改變通常在癌細胞中比較常見,近日來自英國巴布拉漢研究所(Babraham Institute)的研究人員通過研究就發現了一種能夠檢測這些改變的新方法,相關研究刊登于雜志Genome Biology上,該研究或為后期研究人員開發增強癌癥診斷的新方法及癌癥新型靶向療法提供新的思路和希望。
這篇研究報告中,研究者描述了一種名為Hi-C技術的新應用,這種技術能夠幫助研究人員繪制出遺傳物質在細胞內部的排列方式和機制,通過對相關信息進行分析,研究人員就能夠可靠地鑒別出其它方法可能會錯過的一些主要的遺傳改變,相比標準的DNA測序方法而言,這種方法的成本較低。
Hi-C能夠對染色體的重排進行檢測,染色體重排,即大片段DNA發生交換或者在染色體的片段間移動;同時這種技術還能夠對拷貝數變異進行檢測,即遺傳物質的拷貝或剔除情況,所有這些改變都會對細胞的行為產生劇烈的影響。研究者Louise Harewood博士表示,在一般人群和大部分癌癥患者中我們都能夠看到染色體的重排現象,對患者機體的染色體重排進行檢測往往非常麻煩,而且有時候很容易錯過,當然這或許是非常不利的,尤其是在腫瘤學領域中,因為染色體重排往往扮演著診斷和患者預后的角色。
研究者Peter Fraser教授指出,這項研究中,我們對6名腦瘤患者的腫瘤組織進行分析,利用Hi-C技術對癌細胞的基因組進行了檢測,zui終鑒別出了主要的基因組改變;未來這種方法或許就能夠幫助醫生和科學家們在全基因組的廣泛背景下研究遺傳改變,Hi-C技術也將會成為一種強有力的工具幫助理解多種癌癥中復雜的遺傳改變。
zui后,研究者表示,Hi-C技術在檢測染色體異常上扮演著關鍵角色,而且其還能夠幫助發現基因組中的新型融合基因,相比當前技術而言,該技術還能夠對質量較低的樣本進行檢測,同時也能夠通過相同的數據提供拷貝相同的信息,相比當前使用的DNA測序標準方法而言,這種新技術的成本將會大大降低。
4. Cell:2型糖尿病產生新發現!SLC16A11基因變異通過兩種不同的機制破壞其在肝細胞中的功能
doi:10.1016/j.cell.2017.06.011
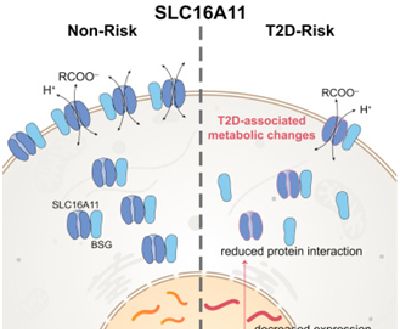
在對早前的針對拉丁美洲人的2型糖尿病(type 2 diabetes, T2D)全基因組關聯研究(GWAS)中的發現進行跟蹤研究后,來自美國布羅德研究所和麻省總醫院等研究人員將這項研究中檢測到的一種關聯性追蹤到一個特定基因(即基因SLC16A11)的變異體上,并且發現這些變異體利用兩種不同的機制破壞該基因在肝細胞中的功能,從而可能導致T2D產生。這些發現對T2D的生物學性質提供新的認識,并且為開發治療這種疾病的藥物提供新的線索。相關研究結果發表在2017年6月29日的Cell期刊上,論文標題為"Type 2 Diabetes Variants Disrupt Function of SLC16A11 through Two Distinct Mechanisms"。論文通信作者為布羅德研究所代謝項目聯合主任、哈佛醫學院副教授、麻省總醫院糖尿病部門主任Jose Florez和布羅德研究所創始主任Eric Lander。論文*作者為布羅德研究所前哈佛醫學院研究生(如今在Jnana治療公司任職)Victor Rusu和布羅德研究所博士后研究員Eitan Hoch。
2型糖尿病是一種影響著身體如何處理血糖的慢性代謝疾病。盡管環境因素在T2D產生中發揮著作用,但是這種疾病也是高度遺傳性的,不過所涉及的遺傳性是復雜的,這是因為很多基因都會導致這種疾病風險。盡管在確定T2D的遺傳構成上已取得進展,但是人們對不同類型的基因變異如何可能導致這種疾病仍然知之甚少。
在*,T2D影響著4億多人,但是對某些人群(比如拉丁美洲裔人群患上這種疾病的可能性是歐洲裔人群的2倍)的影響尤其嚴重。
作為美洲基因組醫學瘦身計劃(Slim Initiative in Genomic Medicine for the Americas)2型糖尿病聯盟(Slim Initiative in Genomic Medicine for the Americas T2D Consortium)的一部分,布羅德研究所糖尿病研究組的研究人員猜測這種影響的不一致性可能有助揭示這種疾病的遺傳學基礎,并且與早前的全基因組關聯研究(GWAS)的合作機構攜手從來自墨西哥和美國的9000多名拉美裔人的DNA樣品中發現了T2D的遺傳決定因子。之前的研究關注歐洲裔人群。
他們取得的發現之一是人基因組的一個特定區域發生的變異與糖尿病風險增加大約30%相關聯。這種變異在非洲不存在,在歐洲比較罕見,但是在美洲較為常見,而且它解釋了拉丁美洲裔人群T2D發生率增加的20%。但是發現一種關聯僅是理解遺傳學在這種疾病產生中發揮作用的*步。
即便關注一個特定的基因也充滿挑戰,在GWAS研究中發現的每個位點橫跨多個基因。2013年,由David Altshuler(如今是Vertex制藥公司的科學家)領導的一項研究已證實存在于這個區域中的基因SLC16A11攜帶著幾種可疑的突變,而且對該區域進行更加詳細的遺傳作圖強化了人們對它的關注。然而,這個基因可能在T2D中發揮的作用仍然是個謎。
這些研究人員在此之前并不知道SLC16A11發揮什么作用,在何處發揮作用。SLC16A11屬于一個已知轉運分子通過細胞膜的基因家族,但是這些基因產生的蛋白能夠在體內發揮著許多不同的作用,它們能夠在一些組織中是有活性的,但在其他的組織中是沒有活性的。他們不僅必須知道SLC16A11如何在正常情形下發揮功能,而且還需確定這個基因發生的突變如何破壞這種功能。特別地,他們需要確定"影響方向(direction of effect)":基因活性是增加還是下降?理解這種功能將會針對這個基因在T2D中的潛在作用提供至關重要的線索。
通過一系列測試,這些研究人員發現SLC16A11基因發生的突變通過兩個不同的機制改變基因活性,而且都是按照相同的"影響方向"破壞這個基因的功能。SLC16A11基因中的一些變異僅是降低它在肝臟(作為一種器官,肝臟有助調節血糖水平,因而參與T2D產生)中的表達。這個基因中的其他變異破壞與另一種被稱作基礎免疫球蛋白(basigin, BSG)的蛋白之間的相互作用。這種破壞改變SLC16A11在細胞中的位置,阻止BSG蛋白發揮著一種轉運體的作用,從而影響脂肪在肝臟中的處理方式。
Rusu解釋道,"為了確定破壞這個基因如何可能在疾病環境下發揮作用,我們采取化學手段敲除SLC16A11在人肝細胞中的活性。我們發現抑制這個基因表達會導致脂肪酸和脂質代謝發生變化,這些變化讓人聯想起我們在胰島素耐受性和T2D中觀察到的情形。"
這些發現提示著恢復SLC16A11功能可能有益于治療T2D,從而為尋找治療藥物打開新的途徑。如果能夠發現,那么這些藥物可能不僅抵抗SLC16A11基因突變產生的影響,而且也潛在地抵抗任何可能通過類似機制觸發這種疾病產生的T2D相關變異。
5. Cancer:新技術可幫助鑒定男性前列腺癌相關基因突變
DOI: 10.1002/cncr.30817
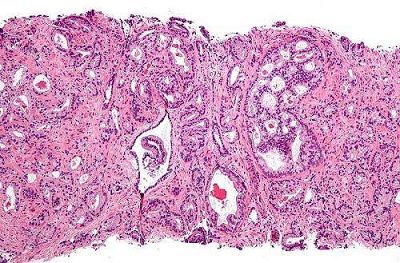
盡管前列腺癌是目前困擾男性的zui嚴重的非皮膚性癌癥,研究者們對于前列腺癌的遺傳背景的了解卻十分有限。來自猶他健康大學的研究者們對前列腺癌患者進行了分析,鑒定出了相關的遺傳突變特征,這些結果或許能夠幫助針對性療法的改進以及評估患者親屬患前列腺癌的風險。相關結果發表在zui近一期的《Cancer》雜志上。
該文章的作者,來自MD安德森癌癥中心的Pilié博士希望能夠基于前列腺患者的個人臨床病史,鑒定出相關的遺傳突變。該研究招募了102名被診斷患有前列腺癌的癌癥患者,他們同時患有至少一種其它類型的癌癥,例如黑色素瘤、胰腺癌、睪丸癌、霍奇金淋巴瘤等等。
利用下一代測序技術,研究者們分析了這群患者生殖系統的相關基因突變的頻率。結果顯示,有11%的患者在至少一類癌癥相關基因中存在突變現象,這表明這一遺傳突變或許導致了癌癥的發生。此外,通過對患者的個人以及家族病史進行分析,發現其中大部分患者(64%)并不滿足遺傳檢測的標準。這一發現表明,目前的遺傳檢測手段并不能夠有效地檢測出攜帶生殖細胞基因突變的前列腺癌患者的具體情況。
"這篇文章描述了通過分析多種癌癥(包括前列腺癌)的臨床病史從而鑒定患者是否攜帶生殖細胞基因突變的方法"。事實上,大部分有害的基因突變都與DNA的損傷修復有關,"這些基因的突變會阻礙DNA的自我修復,從而導致癌癥的發生"。Cooney說道。
"這一研究能夠幫助我們鑒定出具有患前列腺癌高風險的人群,從而指導其盡早地接受診斷與治療"。
6. Nat Genet:單基因突變導致過敏性皮炎的發生
DOI: 10.1038/ng.3898

zui近,研究者們鑒定出了一類導致神經性皮炎發生的關鍵基因突變:CARD11。來自美國NIH過敏與傳染病研究所的研究者們通過對四個沒有血緣關系的患病家庭進行分析,發現了這一導致疾病產生的基因、相關結果發表在《Nature Genetics》雜志上。此外,研究者們還發現通過補充谷氨酰胺能夠緩解該疾病的嚴重程度。
科學家們分析了患有嚴重神經性皮炎的患者以及來自四個家庭中的攜帶CARD11突變基因的成員的基因組序列。他們發現這些志愿者中一些人存在其它的健康問題,但另外一些人則沒有相應癥狀。這說明CARD11的突變引發的神經性皮炎并不一定會導致其它嚴重疾病的發生。
接下來,研究者們希望了解CARD11突變對神經性皮炎產生的具體影響。作者發現,這四個家庭雖然CARD11的突變方式不同(即它們的CARD蛋白發生突變的具體結構域不同),但他們體內的T細胞信號的傳遞都受到了影響。通過細胞培養的試驗,作者發現上述兩條受影響的信號通路在人為添加了谷氨酰胺之后能夠得到恢復。
由于在體外培養這些T細胞的過程中,通過人為添加谷氨酰胺以刺激mTORC1的表達會恢復其中一條受到影響的信號傳遞通路,說明谷氨酰胺治療神經性皮炎具有一定的潛力。如今,研究者們正計劃進行一項有關補充谷氨酰胺以及亮氨酸對于激活mTORC1的試驗,并探究這種方法治療神經性皮炎的效果。
7. Cell:挑戰常規!上千個周圍基因影響大多數疾病
doi:10.1016/j.cell.2017.05.038
在對導致疾病的基因進行研究中,一種核心假設是這些基因簇集在與這種疾病直接相關的分子通路中。但是在一項新的研究中,來自美國斯坦福大學醫學院的研究人員指出事實并非如此。
這些研究人員發現細胞中的基因活性形成一種廣泛的網絡結構以至于幾乎任何一個基因都能夠影響疾病。因此,大多數疾病的遺傳特征并不是歸因于少數核心基因(core gene)而是歸因于來自絕大多數周圍基因(peripheral gene)的微小貢獻。這些周圍基因在致病通路外發揮功能。這似乎表明任何給定的性狀并不是少數基因控制著的。相反,在基因組中,幾乎每個基因都會影響關于我們的一切。這些影響可能是微小的,但是它們產生累積效應。相關研究結果發表在2017年6月15日的Cell期刊上,論文標題為"An Expanded View of Complex Traits: From Polygenic to Omnigenic"。論文通信作者為斯坦福大學醫學院遺傳學教授、生物學教授Jonathan Pritchard博士;博士后研究員Yang Li博士;研究生Evan Boyle。
這些研究人員將他們對致病性基因的易引起爭論的新理解稱為"全基因模型(omnigenic model)",即幾乎任何一個基因都會影響疾病和其他的復雜性狀。Pritchard說,在任何一個細胞中,可能有50~100個核心基因對一種給定的性狀產生直接的影響,而且在這個相同的細胞中表達的另外10000個周圍基因對這種性狀產生間接的影響。
每個周圍基因都對這種性狀產生較小的影響。但是鑒于這些上千個周圍基因在數量上遠遠超過核心基因,大多數與疾病相關的基因變異和其他的性狀是由這上千個周圍基因導致的。因此,諷刺的是,這些對疾病的影響zui為間接和比較小的周圍基因zui終導致大多數的疾病遺傳模式產生。
從多基因模型到全基因模型
Pritchard說,在此之前,他曾認為遺傳上復雜的性狀遵循著一種多基因模型:不論這種性狀是身高或自閉癥等疾病,每個基因都對它產生直接的影響。
但是在去年,當整理一篇針對北歐人近期進化的論文時,Pritchard不得不反思這一觀點。
在早前針對身高遺傳學的研究中,Pritchard和他的同事們吃驚地發現整個基因組實際上都影響身高。他說,"這真地是違反直覺的。老實說,我曾認為這很可能是錯誤的。"他的團隊花了很長時間試圖理解這一令人吃驚的結果。
不過,他說,"我逐漸開始意識到這些數據并不真地符合這種多基因模型。我們開始思考,'如果整個基因組都參與身高等復雜性狀,那么這是如何做到的呢?'"
治療意義
這種多基因模型讓科學家們著重關注在已知影響疾病的分子通路中發揮功能的少數核心基因。因此,治療研究通常意味著解決這些核心基因。一種常見的基因發現方法是開展更大的全基因組關聯研究,但是Pritchard團隊反對這種方法,這是因為更大的樣本量是比較昂貴的,而且發現的這些上千個周圍基因可能具有微小的間接影響。Pritchard說,"在頭100次篩選后,很可能發現通過全基因組研究獲得的大多數核心基因。"
不過,他承認對這些核心基因進行深度測序來找出罕見的變異體可能具有更大的意義。Pritchard說,就臨床應用而言,全基因組關聯研究仍然有其合理性:針對單個病人預測基于周圍基因的風險因素以便開發出個人化療法。
對基礎科學的影響
Pritchard的全基因模型有望給基礎科學研究指出新的方向,而且意味著生物學家們還需要更多地了解將這上千個致病性周圍基因關聯在一起的網絡結構。
8. Sci Adv:什么?特殊基因突變或能促進男性長壽!
DOI: 10.1126/sciadv.1602025

近日,一項刊登在雜志Science Advances上的研究報告中,來自美國、法國和以色列的研究人員通過研究發現,生長激素受體基因突變或能夠使得某些男性壽命變得更長,文章中,研究者對多個不同的男性群體進行研究發現了生長激素受體外顯子3剔除后的差異。
生長激素是能夠連接細胞表面其它分子的特殊分子,其能夠促進細胞加速生長,而且在某些情況下能夠釋放名為生長因子的分子;此前研究中,研究人員通過研究發現,對于某些人而言,機體中存在一種抑制特殊生長因子受體發育的遺傳突變,這種人仍然存在受體,但是形狀卻并不相同;本文中,研究人員希望通過研究來闡明生長激素受體外顯子3的突變剔除情況,通過研究他們還發現,這類男性或許平均能夠多活10年時間,而且平均還能長高一英寸。
文章中,研究人員首先對60歲以上的北歐猶太人人群及其后代(共567名個體)進行研究,他們發現,在100歲以上的人群中,這種突變在12%的人群中都存在,而且攜帶這種突變的人群數量相當于70歲男性的三倍多,攜帶該突變的男性往往能夠比不攜帶的個體而言平均多活10年,但在女性中卻無明顯差異。
研究者表示,這項研究發現在所有研究組中都得到了相同的研究結果,他們認為,外顯子3很明顯和機體長壽直接相關,盡管研究者很樂意承認該基因僅是眾多因子中的一個;但是,如今相關的研究結果卻提示道,后期研究人員還需要在大型的研究人群中來證實本文的研究結果,如果也能夠得到相一致的研究結果,那么后期研究人員將會通過模擬生長激素受體基因的突變來觀察這是否能夠延長男性個體的壽命,并且使得攜帶突變的個體長得高一點。
9. Nat Genet:全基因組關聯性研究闡明誘發肺癌的新型易感位點
doi:10.1038/ng.3892
近日,一項刊登在雜志Nature Genetics上的研究報告中,來自多倫多大學等機構的研究人員進行了一項大型的全基因組關聯性研究,他們利用多個癌癥研究機構所開發的基因分型平臺鑒別出了肺癌的新型易感性位點。
盡管吸煙是引發肺癌的主要風險因子,但過去研究結果表明,肺癌的遺傳性或許占到了18%;當然此前的全基因組關聯性研究中,研究人員也鑒別出了多個肺癌易感位點,但研究者對于大部分疾病遺傳性都無法解釋,本文研究中研究人員就在該項研究上取得了重大突破。
這項研究中,研究人員對有現有數據的歐洲個體進行研究(包括14803名研究對象和12262名對照個體),zui終他們鑒別出了18個疾病易感位點,其中包括10個新型位點;這些新型位點能夠揭示出肺腺癌和鱗狀肺癌兩種肺癌亞型之間風險模式的驚人變化,其中4個位點和總體的肺癌相關,6個位點和肺腺癌直接相關,研究者還發現,和端粒功能相關的多個基因的突變或許在誘發肺腺癌風險上扮演著關鍵角色(并非鱗狀肺癌風險)。
研究者Amos說道,讓我們非常激動的是這項研究的規模以及所發現的影響肺癌風險的基因都是此前其他研究人員并未報道過的;本文研究或能幫助我們闡明影響肺癌風險的新機制;尤其是研究人員鑒別出了多個影響細胞端粒功能的新型突變,這些突變能夠直接影響肺腺癌的風險。
此外,研究者還發現,影響肺癌風險的煙堿性受體亞單位周圍的突變以及吸煙似乎會對機體小腦產生一定的影響,研究人員很少發現小腦能夠參與影響機體的成癮行為;后期研究人員還需要進行更為深入的研究來理解靶向基因在影響肺癌風險、吸煙行為和吸煙效應上所扮演的角色。



