產品搜索
聯系我們
電話:4008750250
手機:18066071954
地址:南京市棲霞區緯地路9號
Email: zhangxiangwen@cobioer.com
新聞動態 / news
黑色素瘤的預防與治療研究進展
原載自:www.diyiqukuai.com.cn[行情動態] 2018-02-28 瀏覽次數:1789
本期為大家帶來的是黑色素瘤的預防與治療領域的研究進展,希望讀者朋友們能夠喜歡。
1. Science:震驚!腸道細菌調節黑色素瘤對免疫療法作出的反應
doi:10.1126/science.aan4236
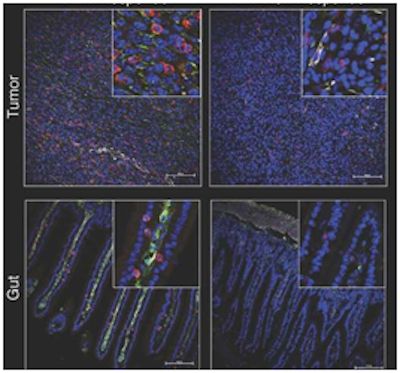
在一項新的研究中,來自美國德州大學MD安德森癌癥中心的研究人員報道生活在人腸道中的細菌能夠如何影響癌癥對免疫療法作出的反應,這為改進治療的研究開辟新的途徑。相關研究結果于2017年11月2日在線發表在Science期刊上,論文標題為"Gut microbiome modulates response to anti-PD-1 immunotherapy in melanoma patients"。 通過分析轉移性黑色素瘤患者的糞便樣品來評估這些患者的腸道微生物組,這些研究人員發現如果這些患者含有更加多樣化的腸道細菌群體或者大量的某些細菌,那么他們接受抗PD1免疫檢查點阻斷治療后能夠在更長的時間內控制他們的疾病。
論文通信作者、德州大學MD安德森癌癥中心外科腫瘤學與基因組醫學副教授Jennifer Wargo博士說,"你能夠改變你的微生物組,這并不難,因此我們認為這些發現開啟了巨大的新機遇。我們對患者開展的研究和隨后的小鼠研究深刻地表明我們的腸道微生物組調節全身免疫和抗腫瘤免疫。"
Wargo和同事們正在與帕克癌癥免疫治療研究所合作開展一項將免疫檢查點阻斷和微生物組調節相結合的臨床試驗。
論文共同*作者Vancheswaran Gopalakrishnan博士說,已有研究證實一個人的微生物組是一種可改變的風險因素,可通過飲食、鍛煉、抗生素或益生菌使用或者糞便移植加以改變。
免疫檢查點阻斷藥物會激活人體自身的免疫系統來攻擊癌細胞,從而讓大約25%的轉移性黑色素瘤患者受益,但是這些免疫治療反應并不總是持久的。
為了評估腸道微生物組的影響,Wargo和同事們分析了接受抗PD1免疫治療的患者的糞便樣品和口腔拭子(buccal swab),其中口腔拭子是來自臉頰內的組織樣品,而抗PD1免疫治療阻斷T細胞表面上的對免疫系統起著抑制作用的PD1蛋白。他們開展16S rRNA測序和全基因組測序來確定口腔拭子和糞便微生物組的多樣性、組成和功能潛力。
盡管這些研究人員發現基于口腔拭子的反應或進展沒有明顯差異,但是對30名對這種抗PD1免疫治療作出反應的患者和13名不作出反應的患者的糞便樣品開展的分析則表現出不同的結果。
(1)具有更高的腸道細菌多樣性的患者擁有更長的中位無進展生存期(progression-free survival, PFS)。中位無進展生存期指的是在某個時間點上,一半接受研究的患者發生疾病進展。盡管具有更高的腸道細菌多樣性的患者并未達到中位無進展生存期(一半以上的患者未發生疾病進展),但是那些具有中度腸道細菌多樣性的患者和那些具有較低腸道細菌多樣性的患者都已達到中位無進展生存期,分別為232天和188天。
(2)對抗PD1免疫治療作出反應的患者和未作出反應的患者的腸道微生物組存在著顯著的組成差異:未作出反應的患者腸道微生物組富含擬桿菌(Bacteroidales),作出反應的患者腸道微生物組富含瘤胃球菌(Ruminococcaceae)。相比于腸道中具有更低糞桿菌(Faecalibacterium,屬于梭菌目瘤胃球菌科)水平的患者(中位無進展生存期為242天),腸道中具有更高糞桿菌水平的患者具有顯著延長的無進展生存期(尚未達到中位無進展生存期)。
(3)腸道中的擬桿菌水平與更快的疾病進展相關聯:相比于腸道微生物組中具有較低的擬桿菌水平(中位無進展生存期為393天),腸道微生物組中具有更高的擬桿菌水平與顯著降低的無進展生存期(中位無進展生存期為188天)相關聯。
進一步的分析表明對抗PD1免疫治療作出反應的患者(腸道中具有較高的有益的梭菌/瘤胃球菌水平)具有更多的T細胞進入到腫瘤中和更高水平的殺死異常細胞的循環T細胞。那些具有更高擬桿菌水平的患者具有更高水平的循環調節性T細胞、髓源抑制性細胞(myeloid derived suppressor cells)和減弱的細胞因子反應,從而抑制抗腫瘤免疫反應。
有益的腸道微生物組也與免疫系統在腫瘤部位上增加的抗原加工和抗原呈遞相關聯。
為了研究其中的因果機制,這些研究人員通過糞便微生物組移植(fecal microbiome transplant, FMT)將來自對抗PD1免疫治療作出反應的患者和不作出反應的患者的糞便微生物組移植到無菌的小鼠中。那些接受來自作出反應的患者的糞便微生物組移植的小鼠具有顯著下降的腫瘤生長和更高水平的有益T細胞和更低水平的免疫抑制性細胞。當接受免疫檢查點阻斷治療時,它們也具有更好的治療結果。
Wargo和他的同事們注意到針對微生物組與癌癥治療之間的關系,仍然有很多需要人們去了解,因此他們敦促人們不要嘗試利用益生菌或其他方法來進行自我治療。
2. Cell Rep:鑒別出促進黑色素瘤進展的關鍵蛋白 有望開發出新型癌癥靶向療法
DOI: 10.1016/j.celrep.2017.11.033

近日,發表在雜志Cell Reports上的一篇題為"Radoslav Janostiak et al. MELK Promotes Melanoma Growth by Stimulating the NF-κB Pathway"的研究報告中,來自耶魯大學的研究人員通過研究發現了一種能夠促進黑色素瘤生長的關鍵蛋白,黑色素瘤是一種惡性的皮膚癌,本文研究或有望幫助研究人員開發治療黑色素瘤的新型靶向療法。
MELK基因能夠編碼一種蛋白激酶,這種激酶能夠對其它蛋白進行修飾,相比正常皮膚組織而言,MELK基因常常會在黑色素瘤患者的樣本中出現過度表達的狀況;文章中,研究人員對人類的黑色素瘤細胞進行分析,闡明了MELK基因如何促進黑色素瘤的生長,以及是否阻斷該基因的活性就能夠有效抑制黑色素瘤生長,從而增強當前療法靶向作用BRAF癌基因的效率。
研究者發現,MELK基因能夠被關鍵的促進黑色素瘤的癌基因所調節,其中就包括BRAF基因。此外,研究人員還發現,MELK基因能調節多種細胞蛋白的修飾,而此前科學家們發現這些蛋白能夠作為BRAF或MEK的關鍵靶點;研究者還需要進行額外的實驗來利用靶向藥物或通過遺傳學技術來闡明,是否MELK基因能夠作為一種有效治療黑色素瘤的潛在治療性靶點。
zui后研究者表示,本文研究結果為我們提供了開發黑色素瘤新型靶向療法的關鍵靶點,后期我們還將通過更為深入的研究闡明這種關鍵促黑色素瘤進展蛋白的具體作用機制,并為未來開發新型療法提供新的研究基礎和線索。
3. Sci Rep:突破!科學家開發出能同時有效診斷淋巴瘤和黑色素瘤的新型檢測技術
doi:10.1038/s41598-017-17027-4
近日,一項刊登在雜志Scientific Reports上的研究報告中,來自喬治亞州立大學的研究人員通過研究利用紅外光譜法開發了一種新型血液檢測技術,或能同時對淋巴瘤和黑色素瘤進行診斷。研究者利用中紅外光譜法分析了來自實驗小鼠機體的血清,隨后將非霍奇金淋巴瘤和黑色素瘤小鼠同健康小鼠成功進行了區分;電磁波譜的中紅外光譜區通常用來在分子水平下對生物性樣本進行特性分析。
研究者表示,紅外光譜法能檢測由非霍奇金淋巴瘤和皮下黑色素瘤誘發的生化改變,這種技術有望作為一種新型的癌癥篩查手段。目前多項研究發現,很多地區種人們患黑色素瘤的發病率不斷上升,在過去10年里,淺膚色人群黑色素瘤的發病率從3%增加到了7%;此外,目前在美國非霍奇金淋巴瘤在所有癌癥中占到了4.3%的比例,然而當前用于癌癥診斷的策略包括組織檢查和活檢,這些手段非常耗時昂貴,且都是侵入性的操作。
開發一種能檢測黑色素瘤和淋巴瘤的快速可靠的檢測手段對于研究者而言非常重要,因為這些癌癥的早期診斷和療法開發或能有效改善患者的生存狀況;在衰減全反射(ATR)采樣模式中的傅里葉變換紅外光譜學技術(FTIR)或能提供比其它震動光譜學技術更高質量且再現性較好的結果。此前研究中,研究人員利用ATR-FTIR光譜學技術開發出了一種診斷潰瘍性結腸炎的簡單快速的血檢技術。
研究者Perera表示,我們的目標就是利用紅外光譜學技術診斷多種疾病,本文研究中我們就利用該技術成功對淋巴瘤和黑色素瘤進行了診斷;盡管本文研究是對小鼠進行的,但該研究結果或許同樣適用于人類機體,因為小鼠和人類共有多種生物標志物和化學物質,此前對結腸炎的研究中,研究者就在患病人類和小鼠機體中鑒別出了特殊的化學物質。本文中,利用收集的淋巴瘤和黑色素瘤生物標志物,研究人員就能針對這些特殊的標志物吸收峰開發出檢測器,這樣臨床醫生就能利用該技術來對患者的血液樣本進行檢測。
在嬰兒期醫生就會開始追蹤檢測患者的血液數據,同時隨著時間推移對其監測來測定患者的血液相關數據是否會發生改變,在對血液樣本進行對比之前和之后,這些數據通常都會被輸入到電腦程序中,利用合適的統計學分析軟件來確定是否兩組數據之間具有顯著性差異,當然了,醫生并不需要進行這樣的統計學分析。
本文研究對于未來科學家們利用體液樣本來開發有效診斷黑色素瘤和淋巴瘤的新型診斷技術至關重要,未來研究者Perera及其同事將會利用來自人類患者的樣本進行紅外光譜分析來對癌癥及其它疾病進行有效診斷。
4. Science:揭示出黑色素瘤抵抗免疫治療之謎
doi:10.1126/science.aao1710
癌癥科學家面臨的一個緊迫的問題就是為什么免疫療法在一些患者中取得了顯著的效果,但對大多數患者是沒有效果的。如今,來自美國達納-法伯癌癥研究所的兩個研究小組獨立地發現了癌細胞中的一種影響著它們是否對被稱作免疫檢查點抑制劑的免疫治療藥物產生抵抗力或作出反應的遺傳機制。這些發現揭示出潛在的新型藥物靶標,并且有可能將免疫治療的益處延伸到更多的患者和更多的癌癥類型。相關研究結果于2018年1月4日在線發表在Science期刊上,論文標題為"A major chromatin regulator determines resistance of tumor cells to T cell-mediated killing"。
這項研究鑒定出黑色素瘤細胞的免疫治療抵抗機制。它是由達納-法伯癌癥研究所的Kai Wucherpfennig博士和Shirley Liu博士領導的。
這個研究小組都發現了對免疫檢查點抑制劑的抵抗作用受到一組調節著DNA在細胞中如何包裝的蛋白發生的變化的嚴格控制。這組被稱作染色質重塑復合物的蛋白是SWI/SNF;它的組分是不同的基因編碼著的,其中包括ARID2、PBRM1和BRD7。SWI/SNF的作用是打開緊密纏繞的DNA片段,這就使得它的藍圖能夠被細胞讀取,從而激活某些基因表達。
在這項研究中,由Wucherpfennig領導的一個研究小組利用基因編輯技術CRISPR/Cas9篩選黑色素瘤細胞基因組中發生的讓腫瘤抵抗免疫T細胞殺傷作用的變化。T細胞在免疫系統對感染和癌細胞產生的反應中發揮著重要的作用。
通過這種篩選,這些研究人員發現了大約100個基因似乎控制著黑色素瘤細胞對T細胞殺傷作用的抵抗性。讓這些基因失活使得這些癌細胞對T細胞的殺傷變得敏感。通過縮小篩選范圍,他們鑒定出SWI/SNF染色質重塑復合物的PBAF亞型參與抵抗免疫T細胞的殺傷作用。
當PBRM1基因在實驗中被敲除時,這些黑色素瘤細胞對T細胞產生的干擾素-γ變得更加敏感,并且作為應答,產生招募更多的抵抗腫瘤的T細胞進入腫瘤中的信號分子。據這些研究人員所稱,PBAF復合物中的另外兩個基因ARID2和BRD7也在一些癌癥中發生突變,而且這些癌癥,如缺乏ARID2功能的黑色素瘤,可能也對免疫檢查點抑制劑作出更好的反應。
這些研究人員注意到這些基因的蛋白產物"代表著免疫治療的靶標,這是因為讓這些突變失活讓腫瘤細胞對T細胞介導的攻擊變得敏感。"他們補充道,發現改變這些靶分子的方法"將會把免疫治療的益處擴大到更大的患者人群,包括迄今為止對免疫療法產生抵抗力的癌癥患者。"
5. JBC:土壤細菌分泌的天然產物或能成為抵御抗黑色素瘤的強大"武器"
doi: 10.1074/jbc.M116.774836
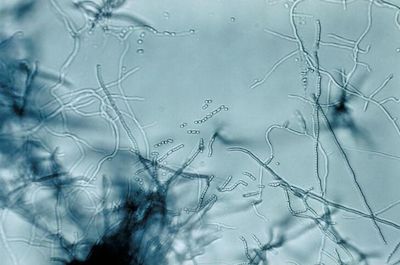
近日,一項刊登在雜志the Journal of Biological Chemistry上的研究報告中,來自俄勒岡州立大學的研究人員通過研究發現,一種土壤中的細菌或能產生誘導黑色素瘤細胞死亡。研究者表示,由波卓鏈霉菌(Streptomyces bottropensis)所產生的次級代謝產物(天然產物)及其特性非常重要,因為其能有效抑制黑色素瘤的生長。
在美國每年有超過8萬名新發黑色素瘤患者,而且有大約9000名患者會死亡,相比女性而言,男性更容易患黑色素瘤,而且黑色素瘤的發病率因種族而異,白種人患病率zui高。研究者Sandra Loesgen教授表示,這種名為mensacarcin的天然產物能夠進入黑色素瘤細胞的線粒體中發揮作用,而線粒體是維持黑色素瘤細胞生長的能量來源。
線粒體對于細胞死亡信號非常重要,因此研究者就希望開發出一種新型的靶向療法,因為癌細胞的線粒體在結構和功能上與非癌變細胞的線粒體并不相同。Loesgen說道,mensacarcin具有強大的抗癌潛力,其能夠選擇性地靶向殺滅黑色素瘤細胞,在美國癌癥研究所的細胞系檢測盤中這種化合物能夠對所有檢測的癌細胞系表現出強大的抗增殖效應,在抑制癌細胞增殖的同時還能使得一部分細胞進入死亡狀態,比如黑色素瘤細胞等。
為了在亞細胞水平下觀察mensacarcin如何對黑色素瘤細胞發揮作用,研究者合成出了一種熒光mensacarcin探針,這種探針能在療法開始的20分鐘內聚集到線粒體中,這種定位能同mensacarcin在黑色素瘤細胞不尋常的代謝效應一起為mensacarcin靶向作用癌細胞的線粒體提供相應證據。活細胞生物能量高通量分析結果表明,mensacarcin能夠干擾癌細胞的能量產生以及線粒體功能,這種化合物的作用方式或許就表明其能作為檢測能量代謝的一種有效探針,隨后的實驗結果表明,mensacarcin能快速改變線粒體的信號通路,從而導致線粒體功能異常;這種異常作用能夠激活細胞凋亡通路。
研究者Loesgen說道,流式細胞術能鑒別出大量發生凋亡的黑色素瘤細胞,而單細胞電泳技術結果表明,mensacarcin能夠引發細胞遺傳不穩定性的發生,這就是早期細胞凋亡的開始,而mensacarcin的*作用方式也表明,其或許有望幫助研究人員開發新型的抗癌藥物。Mensacarcin是一種高度氧化和手性化的復合物分子,其可以通過天然宿主大量獲取,天然產物的發現對于開發新型藥物至關重要,研究者Loesgen在1981至2014年間對新藥進行的一系列分析獲得了美國FDA的批準,其中大約一半小分子藥物制劑都來源于天然產物或其衍生物。
6. Science子刊:溶瘤病毒聯合檢查點抑制劑療法或能有效治療乳腺癌和黑色素瘤
DOI: 10.1126/scitranslmed.aam7577
DOI: 10.1126/scitranslmed.aao1641
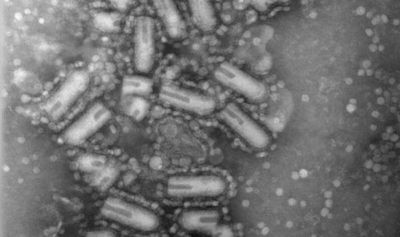
免疫療法能夠幫助機體免疫系統有效抵御癌癥,這種療法為癌癥的治療帶來了革命性的突破,比如治療黑色素瘤和白血病等多種癌癥等,但免疫療法依然無法有效治療很多種類型的癌癥。近日,來自渥太華醫院和渥太華大學的研究人員通過對小鼠進行研究發現,將溶瘤病毒同檢查點抑制劑療法結合的一種新型組合性免疫療法或能有效成功治療乳腺癌及其它多種類型的癌癥,相關成果刊登于雜志Science Translational Medicine上。
研究者Marie-Claude Bourgeois-Daigneault表示,我們很意外地發現利用這種新型組合性療法能夠治愈大部分患癌小鼠,甚至是一些對免疫療法產生耐藥性的小鼠;我們認為,相同的機制在人類癌癥中或許也會發生作用,但后期還需要進行更為深入的研究在人類機體中進行證實。
當前研究中,研究人員重點對三陰性乳腺癌進行研究,這是一種惡性且非常難以治療的乳腺癌。研究者對三只三陰性乳腺癌小鼠模型進行研究發現,這些患癌小鼠對檢查點抑制劑療法均產生了一定的耐藥性,同時他們還發現,當一種名為Maraba的溶瘤病毒在這些患癌小鼠機體中復制時,似乎能幫助小鼠的免疫系統有效識別并且攻擊癌癥,然而單一的溶瘤病毒療法似乎對小鼠的總體生存率影響甚微。
隨后研究者對術后模擬乳腺癌轉移擴散的小鼠模型進行研究,檢測了溶瘤病毒結合檢查點抑制劑療法對模型的作用效果,結果發現,這種組合性療法能治療60%至90%的患癌小鼠,而單獨使用檢查點抑制劑的*為0%,單獨使用溶瘤病毒療法的*也僅有20%至30%,對于這些患癌模型而言,研究人員在術前給予模型病毒治療,同時在術后進行檢查點抑制劑療法治療。
研究者Bell說道,我們的免疫系統會持續識別并且殺滅癌細胞,但癌細胞也總是會嘗試躲避機體免疫系統的識別作用,當將病毒注射到癌細胞中時,似乎就生氣了一面巨大的國旗,其能幫助免疫系統來識別并且攻擊癌細胞;但在某些類型的癌癥中似乎這種方法作用有限,研究者指出,當癌細胞感染病毒后加入檢查點抑制劑療法,其就會釋放所有警報,提醒免疫系統有效攻擊癌癥。
近來研究人員進行的一項臨床試驗也證實,溶瘤病毒和檢查點抑制劑療法聯合后能有效治療黑色素瘤,但本文研究中研究人員證實這種組合性療法可以成功治療乳腺癌;當然這項研究中研究者也嘗試在手術和癌癥轉移模型中檢測病毒和檢查點抑制劑療法的聯合作用效果,對于臨床中患者的治療而言具有重要價值。
7. Nature:重磅!僅利用抗PD-1療法就能有效治療罕見類型的黑色素瘤
doi:10.1038/nature25187
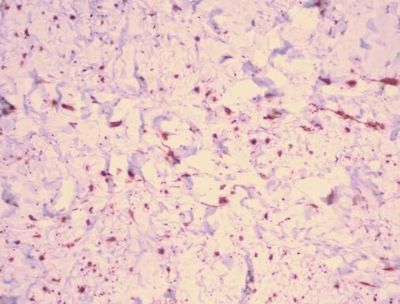
促纖維增生性黑色素瘤(Desmoplastic Melanoma)是日光照射地區人群中zui常見的一種罕見的亞型黑色素瘤,這類黑色素瘤通常很難治療,因為腫瘤會對化療產生耐受性,而且其還缺少一些常見的可靶向作用的突變,而這類突變在其它類型的黑色素瘤中比較常見。近日,一項刊登在雜志Nature上的研究報告中,來自莫非特癌癥研究中心(Moffitt Cancer Center)的研究人員通過研究發現,促纖維增生性黑色素瘤患者或許會對免疫激活的抗PD-1/PD-L1療法表現更為敏感。
重新激活患者自身免疫系統來靶向作用癌細胞的藥物通常會快速變革癌癥療法,派姆單抗和納武單抗就被批準用來治療黑色素瘤,而其它治療性藥物正在開發之中,這些藥物能夠阻斷蛋白PD-1和PD-L1之間的相互作用,在癌癥發生期間,PD-1和PD-L1能夠抑制免疫系統的功能,并且促進腫瘤細胞逃離機體免疫系統的檢測,進而繼續快速生長;通過阻斷這種相互作用,激活免疫系統的藥物或許就能再度刺激免疫系統來檢測并且破壞癌細胞。
此前研究人員認為,促纖維增生性黑色素瘤的組織架構或能降低免疫細胞浸潤到腫瘤區域的能力,并且限制免疫激活藥物的作用效果;然而基于一些正面性的研究結果報道,研究者Zeynep Eroglu等人就假設,促纖維增生性黑色素瘤患者會不會比之前認為的對抗PD-1/PD-L1療法變得反應性更強呢?
為了驗證這種假設,研究人員對此前60名利用PD-1或PD-L1作為靶點進行治療的惡性/轉移性促纖維增生性黑色素瘤患者進行分析研究,他們發現,其中42名患者對抗PD-1/PD-L1療法產生了明顯的反應,大約一半的患者出現了*反應,即患者機體的腫瘤開始*消失了,而且其余患者也出現了部分反應,其機體中腫瘤發生了明顯縮小。在開始治療后74%的患者的存活時間會超過兩年,而能達到70%的反應率也是迄今為止抗PD-1/PD-L1療法所能達到的zui高反應率,這種反應率甚至高于其它類型黑色素瘤患者的治療反應率(大約35%至40%不等)。
隨后研究人員還想通過研究確定為何這些促纖維增生性黑色素瘤患者會因靶向作用PD-1或PD-L1的藥物而獲益,首先他們發現,促纖維增生性黑色素瘤患者機體中DNA的突變水平較高,而且這些突變和日光照射有發的DNA損傷高度相關;NF-1突變就是一種zui常見的遺傳驅動事件;同時研究者還發現,這些黑色素瘤患者機體中會預先存在特殊的免疫細胞和蛋白質來產生抵御癌細胞的免疫反應,他們對比了促纖維增生性黑色素瘤患者和非促纖維增生性黑色素瘤患者的組織活檢特性,結果發現,促纖維增生性黑色素瘤患者機體腫瘤細胞中含有較高水平的PD-L1蛋白,同時患者機體中還含有較高水平的CD8 T細胞,這些細胞對于免疫激活藥物作用的有效發揮非常重要。
研究者Eroglu表示,本文研究結果挑戰了此前科學家們的認知,即由于促纖維增生性黑色素瘤的致密組織架構,免疫療法或許無法有效治療這類黑色素瘤患者,但實際上,這些腫瘤或許攜帶有能被抗PD-1藥物有效靶向作用的生物成分;通常情況下,將兩種免疫療法藥物組合起來就能用來治療黑色素瘤,改善患者的反應率以及生存期;然而相比單一使用抗PD-1療法而言,組合性免疫療法或許也會使得患者出現副作用的發生率明顯提高。本文研究結果表明,單一制劑的抗PD-1療法或許就足以治療促纖維增生性黑色素瘤患者了,如果利用組合性的免疫療法或許還會增加患者的毒性反應。
8. Lancet Oncol:新研究或可改變黑色素瘤的治療手段
DOI: 10.1016/S1470-2045(18)30015-9
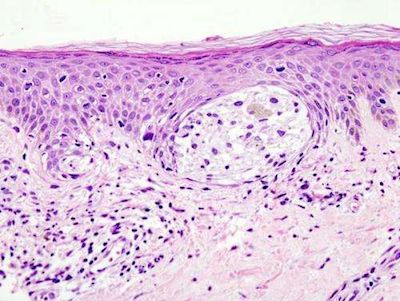
根據zui近由來自羅徹斯特醫學中心的研究者們發表在《The Lancet Oncology》雜志上的一篇文章,目前晚期黑色素瘤患者又多了一種治療選擇。
這項研究比較了兩種不同的治療手段對于高危型黑色素瘤患者(BRAF基因突變)的治療效果,其中一種方案是進行預手術,另外一種方案則是在手術前后接受靶向藥物處理。結果顯示,后一組的患者康復的維持時間相比前一組更久。
"這一結果十分令人興奮,此前還沒有在手術前使用抗癌藥物治療黑色素瘤患者的先例",該研究的作者之一,來自URMC的助理教授Peter Prieto說道:"在這項臨床試驗中,我們不僅發現接受了抗癌藥物療法的患者的治療效果更輕,而且其中58%的患者*沒有復發的跡象"。
目前存在BRAF突變的晚期黑色素瘤患者往往接受了手術切除治療,而僅有不到50%的患者能夠達到五年的存活期。BRAF基因的突變是抗黑色素瘤治療的關鍵(60%以上的患者存在上述突變),十年來研究者們通過靶向BRAF設計藥物改變了黑色素瘤治療的方向。
此前一項小規模的臨床試驗囊括了21名患者,結果表明:手術前后接受兩種藥物(dabrafenib 以及trametinib)治療能夠使患者獲得更久。當然,上述藥物也存在一定的負面作用,例如打冷戰以及頭痛等。
作者稱目前他們仍不清楚需要在手術前多久開始用藥,以及手術后用藥維持的時間為多久,針對這些問題還需要進行下一步的研究。不管如何,這項研究結果表明聯合藥物治療與手術治療能夠極大地改善目前黑色素瘤患者的生存情況。



